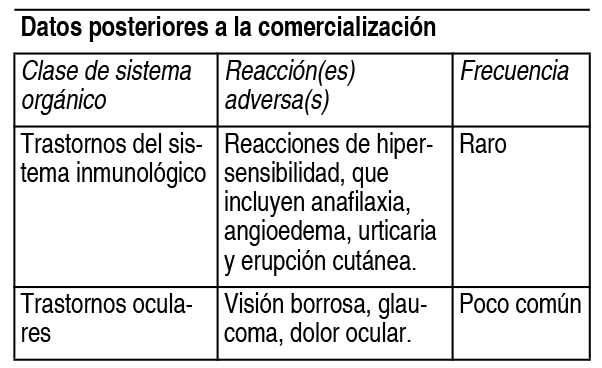
Ver TablaNotificación de sospechas de reacciones adversas: Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio-riesgo del medicamento.
Contraindicaciones: Trelegy Ellipta está contraindicado en pacientes con alergia severa a las proteínas de la leche o que han demostrado hipersensibilidad al furoato de fluticasona/umeclidinio/vilanterol o cualquiera de los excipientes.
Advertencias: No usar para tratamiento agudo: No se dispone de evidencia clínica para apoyar el uso de Trelegy Ellipta en el tratamiento de los episodios agudos de broncoespasmo o para tratar los síntomas agudos del asma o para tratar las exacerbaciones agudas en la EPOC (por ejemplo, como terapia de rescate). Empeoramiento de la enfermedad: El aumento de empleo de broncodilatadores de acción corta para aliviar los síntomas puede indicar un empeoramiento en el control de la enfermedad. En el caso de empeoramiento del asma o de la EPOC durante el tratamiento con Trelegy Ellipta, se debe realizar una reevaluación del paciente y de la posología de tratamiento del asma o de la EPOC. Los pacientes no deben interrumpir el tratamiento con Trelegy Ellipta en asma o EPOC sin la supervisión de un médico ya que los síntomas pueden reaparecer tras interrumpir el tratamiento. Pueden producirse reacciones adversas y exacerbaciones relacionadas con el asma durante el tratamiento con Trelegy Ellipta. Se debe pedir a los pacientes que continúen el tratamiento pero que busquen consejo médico si los síntomas del asma permanecen incontrolados o empeoran después del inicio de Trelegy Ellipta. Broncoespasmo paradójico: La administración de la dosis de furoato de fluticasona/umeclidinio/vilanterol puede causar broncoespasmo paradójico con aparición inmediata de sibilancias y dificultad para respirar que puede poner en peligro la vida. Se debe interrumpir el tratamiento con Trelegy Ellipta inmediatamente si se produce broncoespasmo paradójico. Se debe evaluar al paciente e instaurar un tratamiento alternativo si es necesario. Efectos cardiovasculares: Tras la administración de medicamentos antagonistas de los receptores muscarínicos y simpaticomiméticos, incluido umeclidinio y vilanterol respectivamente, se pueden observar efectos cardiovasculares tales como arritmias cardíacas, por ejemplo, fibrilación auricular y taquicardia. Por lo tanto, Trelegy Ellipta se debe usar con precaución en pacientes con enfermedad cardiovascular inestable o de riesgo vital. Pacientes con insuficiencia hepática: Para los pacientes con insuficiencia hepática de moderada a grave que estén utilizando Trelegy Ellipta, solo se debe utilizar la dosis de 92/55/22 microgramos y se debe monitorizar a los pacientes para detectar reacciones adversas sistémicas debidas a los corticosteroides (véase «Dosificación y administración»: «Posología y farmacocinética»: «Población de pacientes especiales»). Efectos de los corticosteroides sistémicos: Pueden aparecer efectos sistémicos con cualquier corticosteroide administrado por vía inhalatoria, especialmente a dosis elevadas prescritas durante períodos prolongados. La probabilidad de que estos efectos aparezcan es mucho menor que con el uso de corticosteroides administrados por vía oral. Alteraciones visuales: Se pueden producir alteraciones visuales con el uso sistémico y tópico de corticosteroides. Si un paciente presenta síntomas como visión borrosa u otras alteraciones visuales, se debe consultar con un oftalmólogo para que evalúe las posibles causas. Pueden ser cataratas, glaucoma o enfermedades raras, como coriorretinopatía serosa central (CRSC), que se han notificado tras el uso de corticosteroides sistémicos y tópicos. Enfermedades concomitantes: Se debe utilizar Trelegy Ellipta con precaución en pacientes con trastornos convulsivos o tirotoxicosis y en pacientes que responden de forma inusual a los agonistas beta-2 adrenérgicos. Trelegy Ellipta se debe administrar con precaución en pacientes con tuberculosis pulmonar o en pacientes con infecciones crónicas o no tratadas. Actividad anticolinérgica: Trelegy Ellipta se debe administrar con precaución en pacientes con glaucoma de ángulo estrecho o retención urinaria. Se debe informar a los pacientes sobre los signos y síntomas del glaucoma agudo de ángulo estrecho para que dejen de utilizar Trelegy Ellipta y contacten inmediatamente con su médico si presentan alguno de estos signos o síntomas. Neumonía en pacientes con EPOC: Se ha observado un aumento de la incidencia de neumonía, incluyendo neumonía que requiere hospitalización, en pacientes con EPOC que reciben corticosteroides inhalados. Existe alguna evidencia de un mayor riesgo de neumonía con el aumento de la dosis de esteroides, pero esto no ha sido demostrado de manera concluyente en todos los estudios. No hay evidencia clínica concluyente de diferencias intraclase en la magnitud del riesgo de neumonía entre los corticosteroides inhalados. Los médicos deben permanecer vigilantes ante el posible desarrollo de neumonía en pacientes con EPOC, ya que las características clínicas de estas infecciones se superponen con los síntomas de exacerbación de la EPOC. Los factores de riesgo de neumonía en pacientes con EPOC incluyen el tabaquismo actual, pacientes de edad avanzada, bajo índice de masa corporal (IMC) y EPOC grave. Neumonía en pacientes con asma: No se puede excluir una mayor incidencia de neumonía en pacientes con asma que reciben dosis más altas de corticosteroides inhalados. Esto se basa en la experiencia clínica con furoato de fluticasona/vilanterol, donde hubo una tendencia hacia un mayor riesgo de neumonía con furoato de fluticasona/vilanterol 184/22 microgramos, en comparación con furoato de fluticasona/vilanterol 92/22 microgramos y placebo. Hipokaliemia: Los agonistas beta-2 adrenérgicos pueden producir hipocaliemia significativa en algunos pacientes, lo que puede potencialmente producir efectos adversos cardiovasculares. La disminución del potasio sérico es por lo general transitoria, sin que se requiera suplementarlo. A las dosis terapéuticas recomendadas, no se ha observado en los estudios clínicos con Trelegy Ellipta efectos clínicamente relevantes de hipocaliemia. Se debe tener precaución cuando se administra Trelegy Ellipta con otros medicamentos que también puedan causar potencialmente hipocaliemia. Hiperglucemia: Los agonistas beta-2 adrenérgicos pueden producir hiperglucemia transitoria en algunos pacientes. A las dosis terapéuticas recomendadas, no se ha observado en los estudios clínicos con furoato de fluticasona/umeclidinio/vilanterol efectos clínicamente relevantes en la glucosa plasmática. Se han notificado casos de aumento de los niveles de glucosa en sangre en pacientes diabéticos tratados con furoato de fluticasona/umeclidinio/vilanterol, lo cual se debe tener en cuenta cuando se prescriba a pacientes con antecedentes de diabetes mellitus. Una vez iniciado el tratamiento con Trelegy Ellipta, se debe monitorizar más estrechamente la glucosa plasmática en pacientes diabéticos. Excipientes: Este medicamento contiene lactosa. Los pacientes con intolerancia hereditaria a galactosa, deficiencia total de lactasa o problemas de absorción de glucosa o galactosa no deben tomar este medicamento.
Precauciones: Embarazo, fertilidad y lactancia: Embarazo: Hay datos limitados relativos al uso de furoato de fluticasona/umeclidinio/vilanterol en mujeres embarazadas. Los estudios en animales han mostrado toxicidad para la reproducción a exposiciones que no son relevantes clínicamente (véase «Datos de seguridad preclínicos»). Solo se debe considerar la administración de Trelegy Ellipta en mujeres embarazadas si el beneficio esperado para la madre es mayor que cualquier posible riesgo para el feto. Lactancia: Se desconoce si el furoato de fluticasona, umeclidinio, vilanterol o sus metabolitos se excretan en la leche humana. Sin embargo, otros corticosteroides, antagonistas muscarínicos y agonistas beta-2 adrenérgicos fueron detectados en la leche materna. No puede excluirse un riesgo para los recién nacidos lactantes. Se debe decidir si es necesario interrumpir la lactancia o interrumpir el tratamiento con Trelegy Ellipta tras considerar el beneficio de la lactancia para el nińo y el beneficio del tratamiento para la madre. Fertilidad: No hay datos sobre los efectos de furoato de fluticasona/umeclidinio/vilanterol en la fertilidad humana. Los estudios realizados en animales no han mostrado efectos de furoato de fluticasona, umeclidinio o vilanterol sobre la fertilidad femenina o masculina (véase «Datos de seguridad preclínicos»). Efectos sobre la capacidad de conducir y utilizar maquinaria: La influencia de furoato de fluticasona/umeclidinio/vilanterol sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
Interacciones Medicamentosas: Las interacciones clínicamente significativas mediadas por furoato de fluticasona, umeclidinio o vilanterol en dosis clínicas, se consideran poco probables debido a las bajas concentraciones plasmáticas alcanzadas después de una administración inhalada. Interacción con beta bloqueadores: Los bloqueantes beta-2 adrenérgicos pueden disminuir o antagonizar el efecto de los agonistas beta-2 adrenérgicos como el vilanterol. Si se requiere la administración de betabloqueantes, se deben considerar los betabloqueantes cardioselectivos, aunque se debe tener precaución durante el uso concomitante de ambos, betabloqueantes no selectivos y selectivos. Interacción con inhibidores de CYP3A4: Furoato de fluticasona y vilanterol sufren ambos un rápido aclaramiento debido a un intenso metabolismo de primer paso, mediado por la enzima hepática CYP3A4. Se recomienda tener precaución cuando se administra este medicamento junto con inhibidores potentes del CYP3A4 (por ejemplo, ketoconazol, ritonavir, medicamentos que contienen cobicistat), ya que es posible un aumento en la exposición sistémica tanto de furoato de fluticasona como de vilanterol, lo que puede ocasionar un aumento potencial de las reacciones adversas. Se debe evitar la administración conjunta, a menos que el beneficio supere al riesgo aumentado de reacciones adversas sistémicas relacionadas con los corticosteroides, en cuyo caso los pacientes han de estar sometidos a seguimiento para comprobar las reacciones adversas sistémicas de los corticosteroides. Se realizó un estudio de interacción con CYP3A4 a dosis repetidas en sujetos sanos con la combinación furoato de fluticasona/vilanterol (184/22 microgramos) y ketoconazol (400 mg, inhibidor potente del CYP3A4). La administración concomitante aumentó la media del AUC(0-24) y Cmáx de furoato de fluticasona en un 36 % y 33 %, respectivamente. El aumento de la exposición de furoato de fluticasona se asoció con una reducción del 27 % en la media ponderada entre 0-24 horas del cortisol sérico. La administración concomitante aumentó la media del AUC(0-t) y Cmáx de vilanterol en un 65 % y 22 %, respectivamente. El aumento de la exposición de vilanterol no se asoció con un aumento de los efectos sistémicos relacionados con los agonistas beta-2 sobre el ritmo cardíaco o los niveles de potasio en sangre. Interacción con inhibidores del CYP2D6/polimorfismo del CYP2D6: El umeclidinio es un sustrato del citocromo P450 2D6 (CYP2D6). La farmacocinética de umeclidinio, en estado estacionario, se evaluó en voluntarios sanos que carecían de CYP2D6 (metabolizadores lentos). A una dosis 8 veces superior a la dosis terapéutica, no se observaron efectos en el AUC o en la Cmáx de umeclidinio. A dosis 16 veces superiores a la dosis terapéutica, se observó un aumento en el AUC de umeclidinio de aproximadamente 1.3, sin verse afectada la Cmáx del mismo. Con base en la magnitud de estos cambios, no se esperan interacciones medicamentosas clínicamente relevantes cuando se administre conjuntamente furoato de fluticasona/umeclidinio/vilanterol junto a inhibidores del CYP2D6 o cuando se administre a pacientes genéticamente deficientes en la actividad del CYP2D6 (metabolizadores lentos). Interacción con inhibidores de la glicoproteína-P: Furoato de fluticasona, umeclidinio y vilanterol son sustratos del transportador de la glicoproteína-P (P-gp). Se ha estudiado en voluntarios sanos el efecto de verapamilo (240 mg, 1 vez al día) inhibidor de la P-gp moderado, en la farmacocinética en estado estacionario de umeclidinio y vilanterol. No se ha observado ningún efecto de verapamilo sobre la Cmáx de umeclidinio o vilanterol. Se observó un aumento de aproximadamente 1.4 veces en la AUC de umeclidinio sin efecto sobre la AUC de vilanterol. Basado en la magnitud de estos cambios, no se espera ninguna interacción medicamentosa clínicamente relevante cuando se administren conjuntamente furoato de fluticasona/umeclidinio/vilanterol con inhibidores de la P-gp. No se han realizado estudios clínicos farmacológicos con un inhibidor específico P-gp y furoato de fluticasona. Otros antimuscarínicos de larga acción y agonistas beta-2 adrenérgicos de larga acción: No se ha estudiado la administración concomitante de Trelegy con otros antagonistas muscarínicos de acción prolongada o agonistas beta-2 adrenérgicos de acción prolongada y no se recomienda ya que puede potenciar los efectos adversos. Hipocaliemia: El tratamiento concomitante de la hipocaliemia con derivados de metilxantina, esteroides o diuréticos ahorradores de potasio pueden potenciar el posible efecto hipocaliémico provocado por los agonistas β2-adrenérgicos, por lo tanto, se deben usar con precaución.
Sobredosificación: Es probable que la sobredosis produzca signos, síntomas o efectos adversos asociados con la acción farmacológica de los componentes por separado (por ejemplo, síndrome de Cushing, características cushingoides, supresión adrenal, disminución de la densidad mineral ósea, boca seca, alteraciones en la acomodación visual, taquicardia, arritmias, temblor, cefalea, palpitaciones, náuseas, hiperglicemia e hipocaliemia). No hay un tratamiento específico para la sobredosis con Trelegy Ellipta. En caso de sobredosis, el paciente debe recibir tratamiento de soporte y si es necesario, un seguimiento apropiado. Solo se debe considerar la administración de betabloqueantes cardioselectivos cuando se produzcan efectos clínicamente relevantes debidos a una sobredosis grave de vilanterol y que no respondan a las medidas de soporte. Los betabloqueantes cardioselectivos se deben usar con precaución en pacientes con antecedentes de broncoespasmo. Para un manejo adicional se deben seguir las recomendaciones clínicas indicadas o las recomendaciones del Centro Nacional de Toxicología, si estuvieran disponibles.
Incompatibilidades: Ninguna.
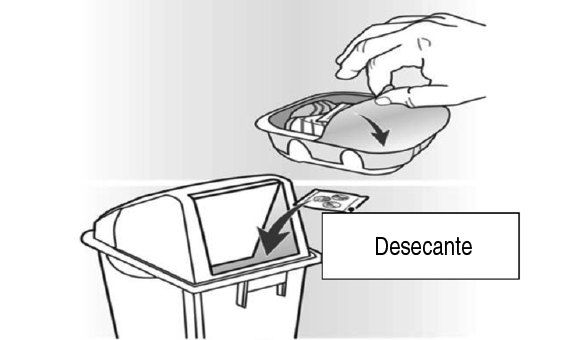
Conservación: Vida útil: La fecha de expiración está indicada en el empaque. Vida útil en uso: Después del retiro de la bandeja, el producto puede almacenarse por un período máximo de: 6 semanas en uso, almacenado a no más de 30 °C. Escriba la fecha en la que debe desecharse el inhalador en el espacio proporcionado en la etiqueta. La fecha debe ańadirse tan pronto como se retire el inhalador de la bandeja. Precauciones especiales de almacenamiento: 24 meses, almacenado a no más de 30 °C. Si se almacena en el refrigerador, deje que el inhalador vuelva a la temperatura ambiente por al menos 1 hora antes de ser utilizado.
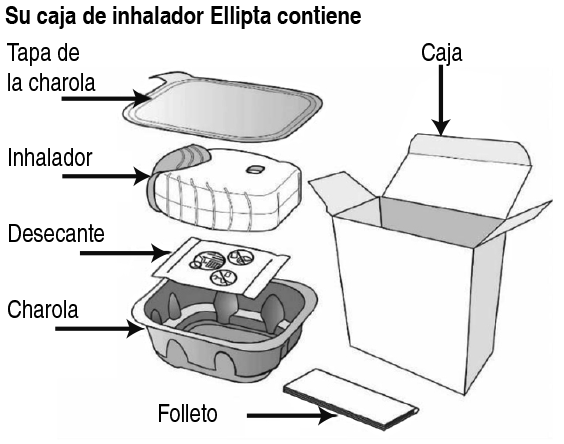
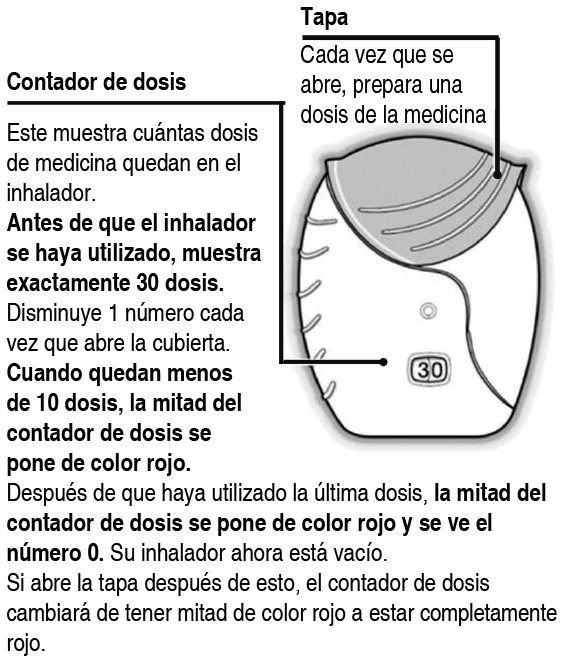
Presentaciones: Naturaleza y contenido del envase: El inhalador plástico de Ellipta consiste en un cuerpo de color gris claro, con una tapa para la boquilla de color beige y un contador de dosis, empacado en una bandeja laminada que contiene un sobre de desecante de silicagel. La bandeja está sellada con una cubierta desprendible. El inhalador contiene 2 tiras de 14 o 30 blísteres, distribuidos de forma regular, los cuales contienen un polvo blanco, cada uno.
 Laboratorio
Laboratorio Laboratorio
Laboratorio Clases Terapéuticas
Clases Terapéuticas Información farmacológica
Información farmacológica
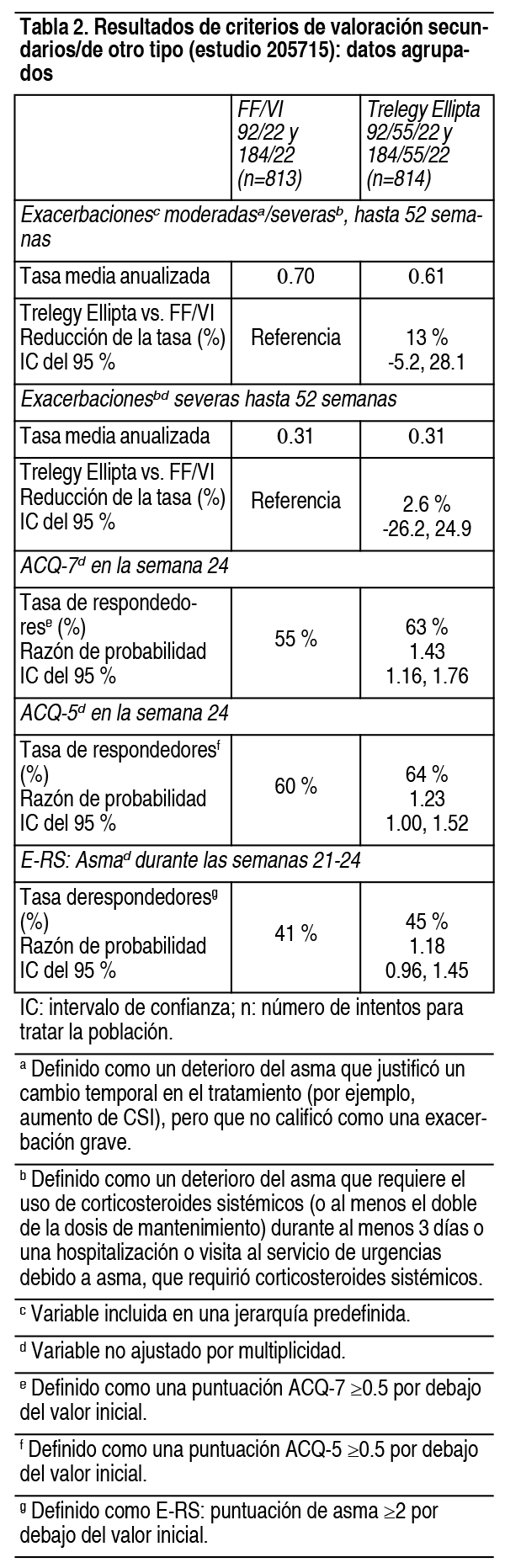
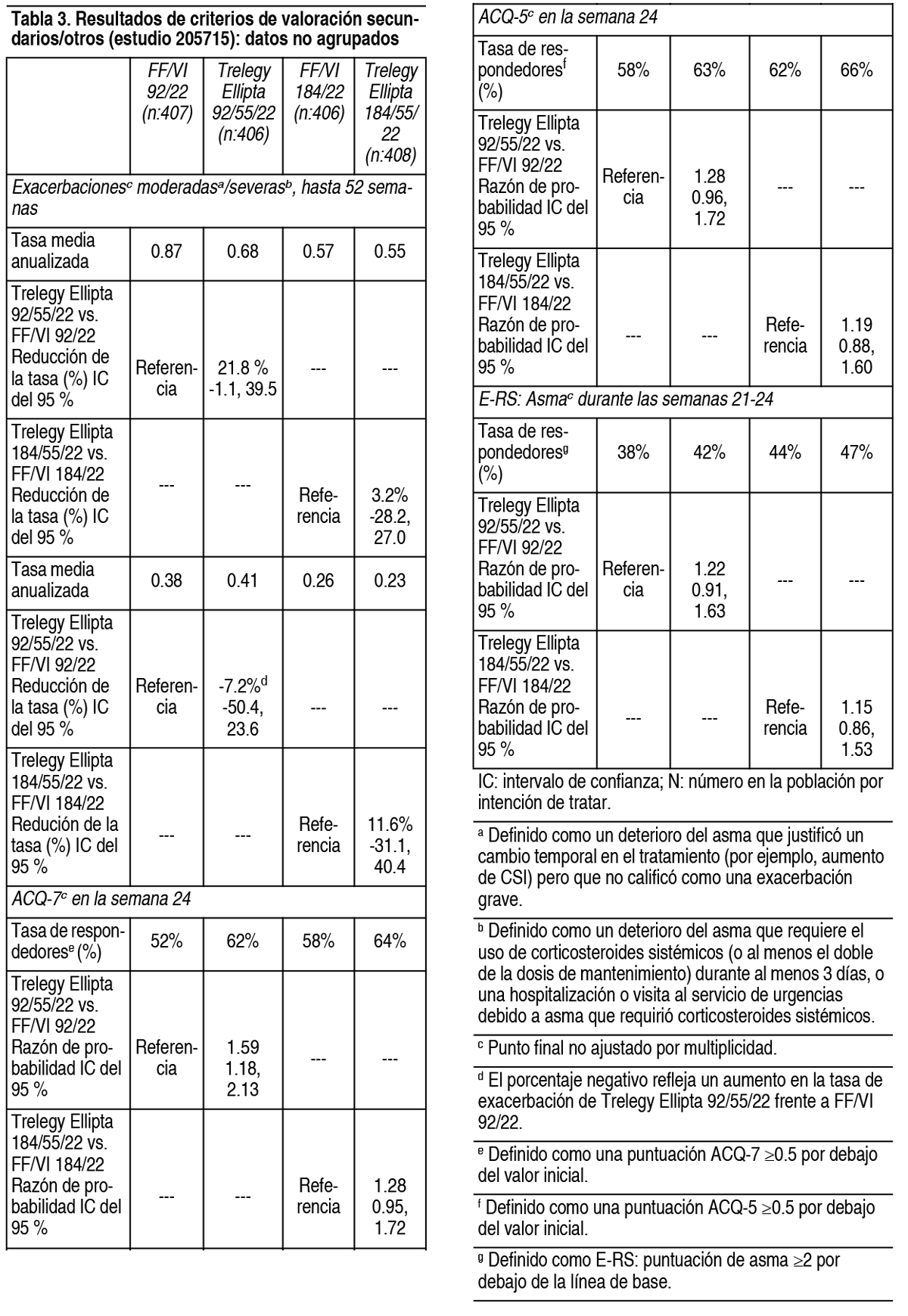
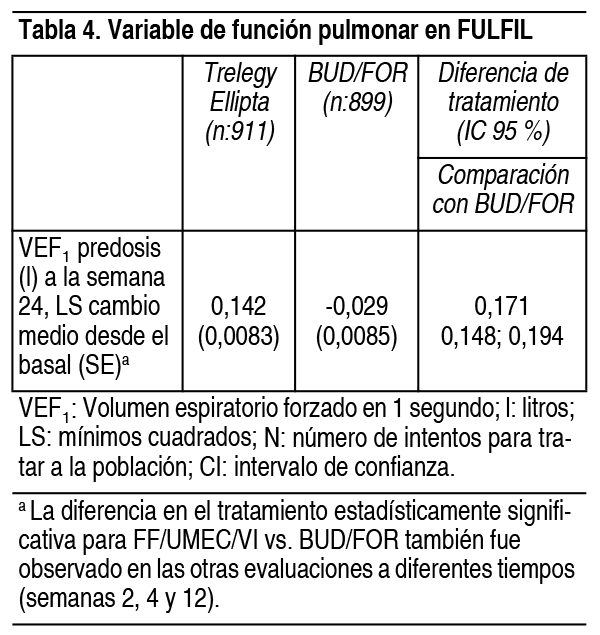
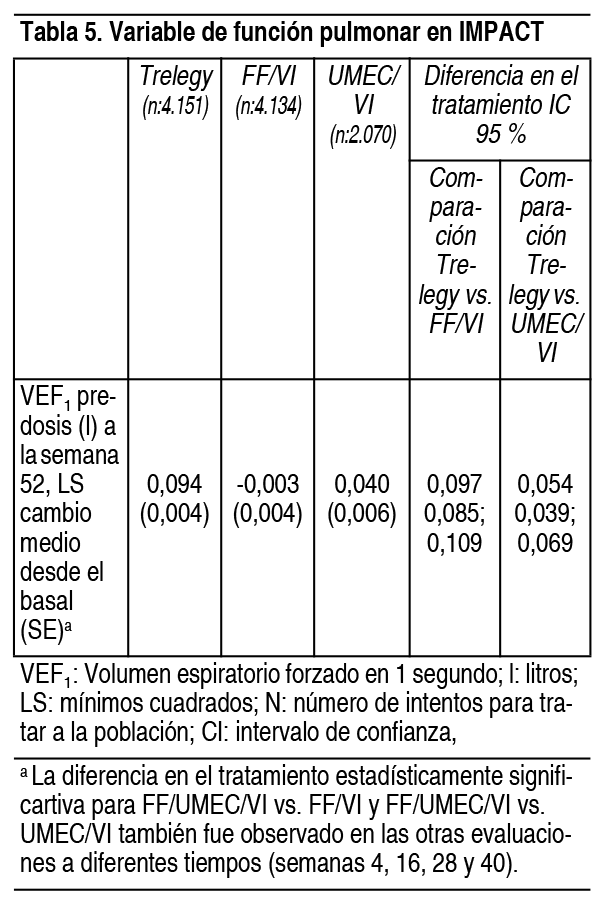

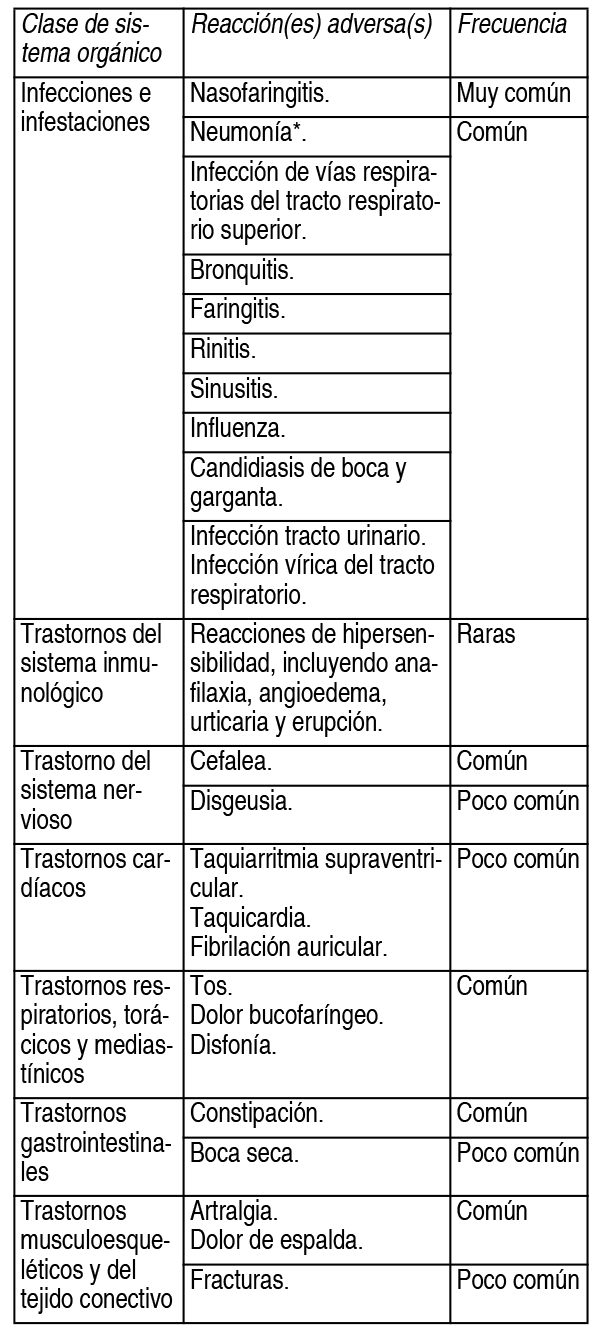
 Ver TablaNotificación de sospechas de reacciones adversas: Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio-riesgo del medicamento.
Ver TablaNotificación de sospechas de reacciones adversas: Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio-riesgo del medicamento.